일산화탄소 중독환자에서 창백핵 병변이 인지기능장애에 미치는 영향
Abstract
Background:
Clinical manifestation of carbon monoxide (CO) poisoning depends on the concentration of CO and duration of exposure. Neurologic presentation is closely related to lesions in the brain.
Case Report:
A married couple suffered from CO exposure from a car engine that was used as a heater during an overnight stay in a cabin. Two weeks later, the wife developed cognitive problems. Neurologic examination was indicative of Gerstmann syndrome. However, her husband was normal. Their brain MRI showed a similar degree of diffuse white matter change. The brain MRI of the wife showed additional lesions in the globus pallidum (GP).
Conclusion:
The duration and amount of CO exposure experienced by the couple was the same, hence the GP lesion had a possible role in the clinical manifestations.
Key Words: Carbon monoxide; Globus pallidus; White matter
서 론
일산화탄소 중독환자의 임상증상은 노출된 농도가 높고 시간이 길수록 그리고 손상된 뇌의 범위가 클수록 심하다[ 1, 2]. 저자들은 한 부부가 같은 일산화탄소 농도와 시간에 노출되었고 손상된 뇌의 범위도 비슷함에도 신경학적 후유증의 정도에서 현저하게 차이가 발생한 증례를 경험하여 보고한다.
증 례
한 부부가 자동차 엔진으로 난방을 하는 오두막에서 하룻밤을 보냈다. 부인은 52세로 다음날 아침 창백한 상태로 발견되었고 깨어난 후 몇 시간 동안 혼돈이 있었다고 했다. 남편은 54세로 당시 경미한 두통 외에 다른 증상은 없었다고 하였다. 부인의 증상은 특별한 치료 없이 회복되었고 이후 일상생활을 하는데 지장이 없었다고 했다. 그러나 약 2 주가 지난 후 부인은 자동차 운전이 미숙해지고 음식을 하는데 지장이 있었다고 하며 집을 찾지 못하고 헤매는 모습을 보여 본원 외래를 방문하였다.
외래 방문 당시 신경학적 검진에서 언어의 경미한 이해능력장애 및 거스트만 증후군(Gerstmann syndrome)을 보였다. 서동, 떨림 등 파킨슨증을 시사하는 이상소견은 없었다. 남편은 기억력이 약간 떨어진 것 같다는 주관적 증상 외에는 호소하지 않았으며 신경학적 검진은 정상이었다.
외래에서 시행한 뇌자기공명영상(Magnetic resonance imaging, MRI)에서는 부부 모두에서 백질의 변성이 뇌실 주위를 중심으로 광범위하게 관찰되었으며 육안적으로 비슷한 정도였다. 부인에서는 양측 창백핵(globus pallidus)에 추가적인 병변이 있었다( Fig. 1). 두 환자의 뇌용적과 백질의 변성 정도를 비교하기 위해 진료용으로 촬영된 뇌 MRI를 정량적으로 분석할 수 있는 Medical Image Processing, Analysis, and Visualization 소프트웨어를 이용하여 전체 뇌의 부피와 백질 변성부위의 부피를 측정하였다. 전체 뇌부피에 대한 백질 변성부위의 부피는 남편에서 9.86%였고 부인에서는 10.46%였다[ 3].
고 찰
본 증례에서 환자들의 초기 증상이 같은 환경에서 잠을 잔 후 발생하였고 초기 증상이 호전된 이후 지연성 뇌손상을 보였다. 자동차 엔진의 경우 불완전 연소로 인한 일산화탄소 중독 사고 위험성 등을 고려하면 초기 증상 발생 당시 검진은 받지 않았으나 환자들의 일산화탄소 중독을 의심하기는 어렵지 않다고 생각된다[ 4]. 뇌자기공명영상 소견에서 창백핵의 병변을 제외하면 성별과 나이의 차이에도 불구하고 백질의 손상 범위는 비슷했다. 이는 일산화탄소의 농도와 노출 시간이 뇌손상의 중요한 요인이라는 이전 연구 결과와 일치하는 소견이다[ 1, 2]. 하지만 체내로 흡수되는 일산화탄소의 양은 노출시간 외에도, 산소의 농도 그리고 분당환기량에도 큰 영향을 받는 것으로 알려져 있다[ 5, 6]. 부인에게 창백핵에 추가적인 병변이 생긴 이유는 정확히 알기 어렵다. 그러나, 성별 또는 체형에 따라 폐활량 등이 달라지고 이로 인해 분당환기량의 차이를 일으켰을 가능성이 있다. 비슷한 환경 조건이지만 신체 조건이 달랐기 때문에 부인의 경우 뇌에 더 많은 일산화탄소가 전달되고, 결국 일산화탄소 중독 손상에 민감한 창백핵에 추가적인 병변을 만들었다고 추정할 수 있다[ 7]. 일산화탄소 중독의 임상증상에 대한 이전 연구에서 인지기능은 뇌 백질 변성과 더 관련이 높다고 보고되었던 반면, 추체외로 증상은 백질의 변성과는 연관관계가 적었다[ 8, 9]. 일산화탄소에 의한 뇌손상과 파킨슨증의 연관성에 대해서는 이 증례와 유사하게 부부가 함께 일산화탄소에 노출된 증례가 보고된 바 있다[ 7]. 두 사람 모두 백질의 광범위한 변성이 있었고 백질 변성 정도는 남편이 좀 더 심했지만 창백핵 병변은 부인에게만 있었다. 기억력 장애와 집중력 장애는 공통적이었으나 창백핵 병변이 없었던 남편에게만 뚜렷한 파킨슨증이 있었다. 이 경우에 부부의 백질 변성 정도가 유사하였으므로 창백핵 병변이 파킨슨증의 발생에 영향을 미쳤을 수 있다. 창백핵절개술(Pallidotomy)을 시행했을 때 파킨슨증이 호전되는 것처럼 양측 창백핵 병변이 일산화탄소 중독에 의한 파킨슨증에 대해서 보호하는 역할을 했을 가능성이 있다. 그러나 창백핵 병변이 있는 일산화탄소 중독환자에서 파킨슨증에 대한 보고가 많아 이러한 추론은 일반화하기 어렵다[ 10]. 우리 증례에서 창백핵 병변은 부인에게만 있었으며 인지기능 장애는 동반되었으나 파킨슨증은 동반되지 않았다. 부부 사이에 백질의 변성 정도는 부인에게 조금 심했지만 (0.6%), 가장 두드러진 차이가 있는 병소는 창백핵이었다. 따라서 임상 증상의 차이를 창백핵 병변과 연관시키는 것은 어렵지 않아 보인다. 그러나, 보통의 MRI에서 보이는 병변이 모두 동일한 정도의 손상에 의한 것이 아닐 수 있다. 따라서 spectroscopy 등 뇌기능을 평가할 좀 더 자세한 검사가 시행되지 않았던 것은 창백핵의 독립적 역할에 대한 해석에 제한점이라고 할 수 있다[ 11]. 부인의 인지기능은 일상생활의 명백한 장애와 신경학적 검진에서 분명하게 파악되었으나 자세한 신경심리검사를 시행하여 정량화된 자료를 얻지는 못했다. 운전, 요리 등의 행동 장애는 계획, 실행 기능에 장애가 있었던 것으로 추정할 수 있다. 창백핵은 기저핵시상피질회로(basal ganglia-thalamocortical circuits)의 주요 구성요소로, 인지기능의 피질하 조절(subcortical control), 특히 전두엽수행기능과 밀접한 관련이 있는 것으로 알려져 있어 창백핵의 병변과 환자의 임상증상에 인과관계가 있을 가능성이 있다[ 12]. 또한, 본 증례에서 남편의 경우처럼 주관적인 기억장애에만 머물 수 있었던 광범위한 백질의 변성에 대한 뇌의 보상상태의 균형이 부인의 경우 추가적인 창백핵의 병변으로 인해 무너져, 길을 찾지 못하는 증상, 거스트만 증후군, 경미한 언어능력의 장애 등의 추가적인 인지기능의 장애가 나타났다고 할 수 있다.
Figure 1.
Brain MRI. T2 fluid attenuation inversion recovery images show similar confluent high signal intensities in periventricular white matters of both patients (A-1, wife; B-1 husband). Focal lesions are located in the globus pallidus (GP) of the wife (A-2) while no lesions in GP of the husband (B-2). 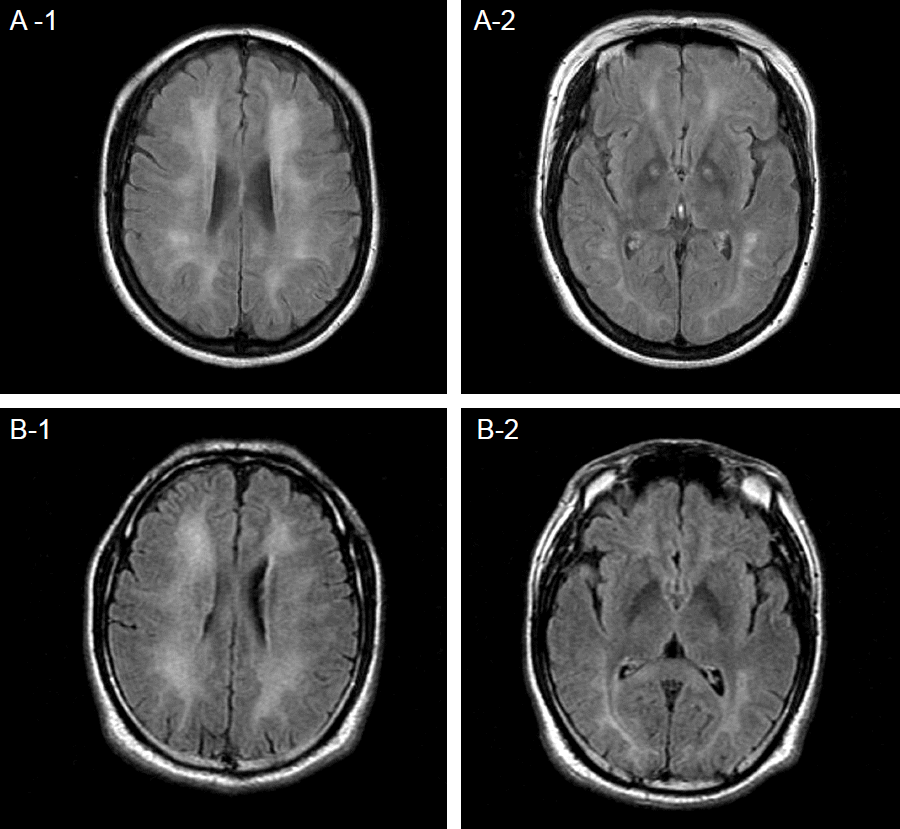
REFERENCES
1. Weaver LK. Clinical practice. Carbon monoxide poisoning. N Engl J Med 2009;360:1217-25.   2. O’Donnell P, Buxton PJ, Pitkin A, Jarvis LJ. The magnetic resonance imaging appearances of the brain in acute carbon monoxide poisoning. Clin Radiol 2000;55:273-80.   4. Vevelstad M, Morild I. Lethal methemoglobinemia and automobile exhaust inhalation. Forensic Sci Int 2009;187:e1-5.   5. Ilano AL, Raffin TA. Management of carbon monoxide poisoning. Chest 1990;97:165-9.   6. Olson KR. Carbon monoxide poisoning: mechanisms, presentation, and controversies in management. J Emerg Med 1984;1:233-43.   7. Lo CP, Chen SY, Lee KW, Chen WL, Chen CY, Hsueh CJ, et al. Brain injury after acute carbon monoxide poisoning: early and late complications. AJR Am J Roentgenol 2007;189:W205-11.   8. Parkinson RB, Hopkins RO, Cleavinger HB, Weaver LK, Victoroff J, Foley JF, et al. White matter hyperintensities and neuropsychological outcome following carbon monoxide poisoning. Neurology 2002;58:1525-32.   9. Choi IS, Cheon HY. Delayed movement disorders after carbon monoxide poisoning. Eur Neurol 1999;42:141-4.   10. Lee MS, Marsden CD. Neurological sequelae following carbon monoxide poisoning clinical course and outcome according to the clinical types and brain computed tomography scan findings. Mov Disord 1994;9:550-8.   11. Sohn YH, Jeong Y, Kim HS, Im JH, Kim JS. The brain lesion responsible for parkinsonism after carbon monoxide poisoning. Arch Neurol 2000;57:1214-8.   12. Alexander GE, Crutcher MD, DeLong MR. Basal gangliathalamocortical circuits: parallel substrates for motor, oculomotor, “prefrontal” and “limbic” functions. Prog Brain Res 1990;85:119-46.  
|
|






